Химические классы пестицидов
Оглавление
- История
- Действие на вредные организмы
- Механизм действия
- Симптомы поражения
- Поражаемые виды
- Резистентность
- Профилактика резистентности
- Замена пиретроидам
- Фитотоксичность
- Применение
- В сельском хозяйстве
- В ЛПХ
- Токсикологические характеристики
- В воде
- Для теплокровных
- В организм человека
- Симптомы отравления
- Острые отравления
- Классы опасности
Пиретроиды сходны по строению структурной формулы и механизму действия с пиретринами (природными пиретроидами). Природные пиретроиды (пиретрины) содержатся в цветках пиретрума (далматской ромашки)[8]. Подробнее – в статье «Пиретрин».
По структурной формуле большинство пиретроидов представляют собой эфиры 3-замещеной -2,2 диметилциклопропанкарбоновой (хризантемовой) кислоты или изостерической кислоты, потерявшей пропановый цикл и соответствующего спирта, содержащего одну или две ненасыщенные связи[1].
Пиретроиды широко распространены в качестве действующих веществ инсектицидов для борьбы с вредителями плодовых и огородных культур, вредителями запасов продовольствия в быту, для обработки сельскохозяйственных животных против эктопаразитов[9].
Преимуществами пиретроидов являются следующие свойства:
- селективная токсичность (селективность);
- возможность модификaции каждой части молекулы при сохранении активности;
- сохранение высокой инсектицидной эффективности и минимальной токсичности для рыб;
- возможность создания почвенных инсектицидов и эффективных фумигантов[8].
Кроме того, синтетические пиретроиды – липофильные вещества, хорошо удерживаются кутикулой листьев и, ограниченно проникая в них, обеспечивают глубинное инсектицидное действие[5].
Одним из самых распространенных пиретроидов в настоящий момент является циперметрин и его изомеры[5].
История
Высушенные цветки некоторых видов ромашки использовались в качестве инсектицида еще воинами Александра Македонского, затем в древнем Китае и в средние века в Персии. Началом научных исследований этих веществ можно считать 1694 г., когда впервые были описаны растения далматской, или пепельнолистной, ромашки, произрастающей на Кавказе и в Далмации (район Югославии)[6].
Позже было установлено, что цветки нескольких видов ромашки (род Chrysanthemium семейства Asteraceae – сложноцветных) обладают инсектицидными свойствамй, но далматская ромашка (Chrysanthemium cinerafolis или Pyrethrum cinerariifolium) соцветия которой содержат до 1,5% пиретрина, нашла наибольшее распространение[6].

Инсектицид "Убийца летающих" против бытовых летающих насекомых, выпускавшийся в 30-40-х годах прошлого столетия. Содержал вытяжку Пиретрина 1 и Пиретрина 2, о чем свидетельствует надпись на упаковке.
Использовано изображение:[14]
В Европе высушенные и измельченные соцветия (пиретрум), обладающие замечательным свойством убиватъ тараканов, клопов, мух и комаров, стали известны более 200 лет назад благодаря торговцам из Армении, которые продавали их как персидский порошок (“Persian dust”, “insect powder”). Далматская ромашка была введена в культуру и успешно выращивалась в Японии, Бразилии и США. С 1890 г. в Японии началось производство москитных палочек, а впоследствии спиралей, которые долго горели и отпугивали мошек. К 1938 г. в мире производили около 18 тыс. т сухих цветков в год, из них около 70% в Японии[11].
Химическое изучение факторов инсектицидной активности пиретрума начато в 1908 г. В 20-х годах XX столетия было доказано наличие циклопропанового кольца в молекулах пиретрума и установлена структура пиретрина I и пиретрина II. Найдено, что инсектицидные компоненты цветков пиретрума содержат шесть кетоэфиров хризантемовой и пиретриновой кислот, очень схожих структурно и определяющих инсектицидную активность пиретрума[11].
В 30-х годах XX столетия на основе извлечения пиретринов органическими растворителями из цветков ромашки начато производство препаратов пиретрума – вязких, тяжелых, белых масел почти без запаха, нерастворимых в воде и содержащих от 2–10 до 90% смеси пиретринов. Пиретрины использовали в основном для борьбы с бытовыми насекомыми и вредителями запасов. Препараты были безвредны для человека и животных, но дороги в производстве, нестойки и быстро теряли инсектицидную активность[11].
Синтез пиретроидных инсектицидов начали в конце 40-х годов. В 1949 г. впервые был синтезирован пиретроид аллетрин, в 1945 г. – тетраметрин, в 1967 г. – ресметрин. На мировом рынке пестицидов в начале 1970-х годов эти первенцы имели серьезный недостаток – относительно быстро теряли активность во внешней среде[7][8].
Определяющее значение на дальнейшее направление синтеза новых пиретроидов оказало исследование механизма их инсектицидного действия. В результате дальнейших исследований по синтезу пиретроидов, проведенных на Ротердамской опытной станции (Англия), был создан высокоактивный и стабильный во внешней среде препарат NRDC-143 (перметрин), полученный включением в молекулу пиретрина I дихлорвинилциклопропанкарбоксиловой кислоты[7].
В СССР изучение пиретроидных соединений впервые начали в ВИЗРе в 1977 г[7].
Красные стрелки указывают на напрвление воздействия.
Использовано изображение:[13]
Действие на вредные организмы
Пиретроиды и пиретрины обладают высокой инсектицидной, часто и акарицидной активностью. Характеризуются контактно-кишечным действием. Высокая липофильность обеспечивает им мгновенное проникновение через покровы насекомых[3].
На активность пиретроидов большое влияние оказывает температура окружающего воздуха. При этом отрицательный температурный коэффициен – увеличение активности при понижении температуры – характерен для пиретроидов первого поколения или тип I (летучих). К ним относятся аллететрин, биоаллетрин, эсбиотрин, эсбиол, праллетрин, трансфлутрин, вапортрин, метофлутрин. В конце 80-х годов европейскими учеными было установлено, что при понижении температуры на 5°С, активность соединений первого поколения пиретроидов увеличивается более чем в три раза. Этот эффект снижается при повышении температуры[1].
Пиретроиды второго поколения или тип II (циперметрин и его изомеры, цифлутрин, цигалотрин (его изомер лямбда-цигалотрин), дельтаметрин, фенвалерат, в отличие от предыдущей группы, имеют положительный "температурный коэффициент". Эффективность этих соединений возрастает с повышением температуры[1].
Одновременно отмечается, что единого мнения по этому вопросу пока не существует, поскольку природа происхождения "температурного коэффициента" пока недостаточно изучена[1]
Механизм действия
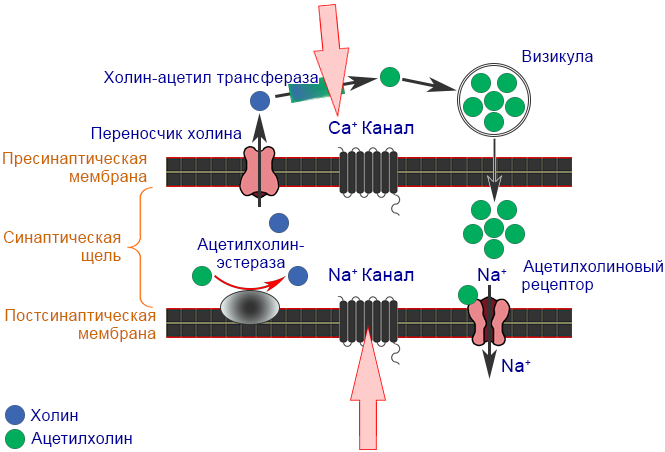
. Пиретроиды и пиретрины действуют на нервную систему насекомых и являются соединениями нервнопаралитического воздействия[1].Согласно классификации IRAC, пиретроиды относятся к группе 3, объединяющей вещества по механизму действия на вредителей являющиеся модуляторами натриевых каналов/sodium channel modulators[12].
К группе 3 классификации IRAC относятся 42 соединения классов пиретрины, пиретроиды (подгруппа A), ДДТ и метоксихлор. Последние два соединения выделены в отдельную подгруппу B[12].
При попадании в организм членистоногих вредителей пиретрин и пиретроидные соединения связываются с липофильным окружением мембраны со стороны внутренней створки натриевого канала нервных клеток. Результатом этого процесса является деполяризация мембраны и замедление закрытия или открытия натриевого канала. Скорость тока ионов натрия в таком модифицированном пиретроидным соединением канале зависит от свойств этого конкретного вещества[11].
Деполяризующее истечение ионов натрия вызывают пиретрин и все пиретроиды. Но наиболее эффективны в этом случае соединения, содержащие в спиртовом комплексе циангруппу. Это фенвалерат, циперметрин, дельтаметрин. По характеру действия они классифицированы как пиретроиды II типа. Деполяризация чувствительных нейронов уже вызывает повторные разряды и обуславливает синаптические нарушения[11].
В отличии от пиретроидов типа II, пиретроиды типа I (аллетрин, тетраметрин) вызывают повторные разряды в пресинаптическом нерве в связи с последующим увеличением деполяризованного потенциала до порога его генерации[11].
Эти эффекты достигаются очень низкими концентрациями пиретроидов (порядка 10−9–10−12 М), модифицирующими только незначительные участки (менее 1%) натриевого канала. Этого достаточно для нарушения нормального функционирования натриевого канала нервных клеток, возникновения нарушений нервной проводимости и деятельности различных областей нерва и мускульной системы[11].
Симптомы поражения
, вызываемые нарушение деятельности нервной системы под воздействием пиретроидов проявляются последовательно как повышенная двигательная активность, нарушение координации движения, конвульсии, прострация, паралич, смерть[8].Поражаемые виды
. Пиретроиды и пиретрины обладают широким спектром действия. Многие характеризуются не только инсектицидной, но и акарицидной активностью. Круг поражаемых видов во много зависит от свойств конкретного соединения[8] В отличие от фосфорорганических инсектицидов и карбаматов пиретроиды и пиретрины не уничтожают скрытоживущих вредителей и применяются чаще всего против листогрызущих насекомых[3].Химические классы и соединения, по механизму действия – модуляторы натриевых каналов (Группа 3 по классификации IRAC):
А. Класс – пиретроиды, пиретрины:
Действующие вещества:
- Аллетрин;
- Альфа-циперметрин;
- Бета-циперметрин;
- Бета-цифлутрин;
- Бифентрин;
- Вапортрин;
- Гамма-цигалотрин;
- Дельтаметрин;
- Зета-циперметрин;
- Лямбда-цигалотрин;
- Перметрин;
- Пиретрин;
- Праллетрин;
- Тау-флювалинат;
- Тетраметрин;
- Тефлутрин;
- Циперметрин;
- Цифлутрин;
- Эсфенвалерат[12].
В. Класс – ХОС:
Действующие вещества:
Резистентность
. Длительное применение пиретроидов и пиретрина на одной и той же популяции вредителей вызывает, как правило, появление резистентных (устойчивых) к данному веществу рас. Природа формирования резистентности вредителей в данном случае основана на том, что пиретроиды и пиретрины в организме насекомых подвержены действию окислительных ферментов и ферментов гидролизующих сложноэфирные группы (эстераз)[11].Действие эстераз приводит к расщеплению исходной молекулы пиретроидного соединения на кислотный и спиртовой компоненты и полной потере инсектицидной активности. Отмечено, что действие ферментов окисления и эстераз направлено на вполне определенные части молекул пиретроидов[11].
Появление резистентных к пиретроидам рас связывают в том числе и с повышением активности указанных групп ферментов. Установлено, что у резистентных насекомых ферментов детоксикации эффективнее дезактивируют поступающие в организм отравляющие вещества[11].
Уровень резистентности может достигать десяти тысяч, что означает, что для уничтожения резистентных по отношению к какому-нибудь инсектицидному веществу вредителей нужно использовать в десять тысяч раз больше вещества в сравнении с обычными насекомыми[5].
Также нередко проявляется кросс-резистентность, при которой применение препаратов на основе одного действующего вещества приводит к появлению рас насекомых устойчивых не только к этому, но и к другим действующим веществам. Преодоление резистентности является серьезной проблемой[5].
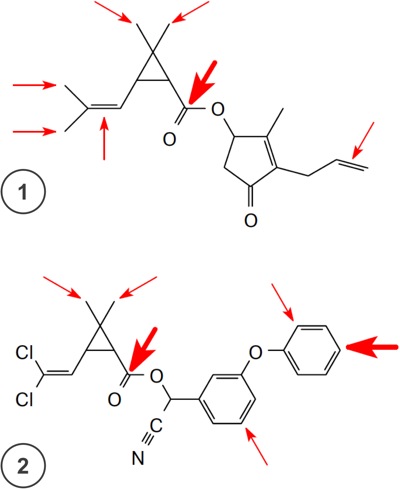
Направления атаки ферментов, приводящей к дезактивации пиретроидов в живом организме. Стрелками показаны места гидролиза при действии эстераз и гидроксилирования (внедрения атома кислорода по связи С–Н) или эпоксидирования с по- следующим окислением и расщеплением. Толщина стрелок отражает относительную значимость того или иного направления атаки:
1 - Аллерин; 2 - Циперметрин.[11]
Профилактика резистентности
. Соблюдение определенных правил при использовании инсектицидных препаратов позволяет снизить риск формирования устойчивых популяций вредителей:- При подборке схемы обработок необходимо чередовать инсектициды, подбирая препараты с действующими веществами разного механизма действия (разных групп по классификации IRAC). В частности, при использовании пиретроидов недопустимо их чередование с препаратами действующим веществом которых является ДДТ или метоксихлор[5][12].
- При подборе схемы обработок следует отдавать предпочтение комбинированным препаратам, включающим в состав соединения различного механизма действия[5].
- Не ограничиваться только химическими методами борьбы. Сочетание агротехнических, химических и биологических мер – наиболее эффективный способ регулирования численности вредителей[5].
- Соблюдение регламента применения пестицидов, при обязательном соблюдении норм расхода[5].
Формированию резистентности к пиретроидам препятствует добавление в инсектицид соединения являющегося синергистом. В данном случае это такие вещества, которые способны дезактивировать (ингибировать) ферменты окисления и эстеразы. Обычно такие вещества не обладают инсектицидной активностью (или она значительно меньше чем у пиретроидов). Примеры подобных соединений:
- пиперонилбутоксид – ингибитор оксидаз;
- профенофос – ингибитор эстераз[11].
Установлено, что добавление пиперонилбутоксида в четыре раза повышает эффективность фенфалерата в отношении колорадских жуков. Профенофос – приводит к 20-кратному усилению действия циперметрина на мух[11].
Замена пиретроидам
В случае наличия у популяции резистентности к соединениям класса пиретроиды или, если говорить о механизме действия, резистентности к соединениям – модуляторами натриевых каналов, эффективным будет применение соединений с любым другим механизмом действия[1].
Предпочтительно сменить их ингибиторы ацетилхолинэстеразы (АХЭ) – ФОС, при отсутствии – на карбаматы. Если ФОС или карбаматы недоступны, рекомендуется применять соединения с механизмом действия ингибиторы синтеза хитина (Группы 15 (бензоилмочевины) и 16 (бупрофезин) классификации IRAC)[1][12].
Применение фенилпиразолов (блокаторы ГАМК-зависимых хлоридных каналов), в случае возникновения резистентности к пиретроидам, рекомендуется избегать или применять их в последнюю очередь, поскольку они, как и пиретроиды, в отдельных случаях, воздействуют и на хлорионные каналы мембран нервных клеток насекомых[1].
В любом случае, при включении того или иного соединения в схему обработок необходимо прежде всего выяснять его механизм действия на вредителей, поскольку часто одно и то же соединение может одновременно относится к разным химическим классам[12].
Фитотоксичность
. Пиретроиды не фитотоксичны[8].Применение
В сельском хозяйстве
. По сравнению с природными пиретринами современные синтетические пиретроиды имеют более высокую инсектицидную активность, фотостабильность, медленнее дезактивируются в организме насекомых, что делает возможным применение их для защиты сельскохозяйственных растений[11].В ЛПХ
. В личном приусадебном хозяйстве используются препараты на основе перметрина, дельтаметрина, циперметрина, альфа-циперметрина, зета-циперметрина, эсфенвалерата[4].Токсикологические характеристики
Пиретроиды относительно стабильны на солнечном свету, на неживых поверхностях могут сохраняться до одного года (перметрин). Они слабо передвитаются в почве, под действием микрофлоры разрушаются в течение 2–4 недель, почти не проникают в растения. Их период полураспада (ДТ50) на поверхности растений составляет 7–9 дней, остатки обнаруживаются в течение 20–25 дней[8].
Благодаря липофильности вещества хорошо удерживаются кутикулой листьев и не смываются дождем, а низкое давление паров обеспечивает длительное остаточное действие и препятствует распространению пиретроидов в окружающей среде воздушными потоками. Эти же физические свойства ограничивают подвижность пиретроидов в почве: благодаря хорошей адсорбции распространение пиретроидов возможно лишь при эрозии почвы[8].
В воде
. Пиретроиды почти нерастворимые в воде. Липофильность и нерастворимость обусловливают высокую токсичность веществ в отношении насекомых и отсутствие системного действия (пиретроиды – это контактные, отчасти кишечные токсиканты). Продукты расщепления пиретроидов на свету имеют пониженную биологическую активность. Практически достаточная устойчивостъ пиретроидов в окружающей среде сочетается с их быстрой инактивацией (благодаря расщеплению) в системе метаболизма[6].При введении в организм животных пиретроиды попадают в жировые отложения и мозг, причем из жировых тканей они выводятся на протяжении 3–4 недель, а из мозга – значительно быстрее. Пиретроиды выводятся из организма тем быстрее, чем токсичнее препарат[6].
Для теплокровных
пиретроиды менее токсичны, чем инсектициды других групп. Это обусловлено тем, что они либо сразу элиминируются, либо метаболизируются (благодаря лабильности эфирной связи), после чего выводятся из организма, а эстеразы, гидролизующие пиретроиды, в печени теплокровных гораздо более активны, чем у насекомых[8][11].Кумулятивные свойства выражены слабо, исключение составляет дельтаметрин[8].
В организм человека
действующие вещества могут поступать через дыхательные пути, желудочно-кишечный тракт, неповрежденную кожу. В печени пиретроиды подвергаются окислению и гидролизу с образованием глюкуронатов. Высокая скорость окисления и выведения этих веществ из организма обусловлена наличием в их молекуле легко расщепляющихся структур[10].Симптомы отравления
. По токсическому действию синтетические пиретроиды делят на два типа. К І типу относятся вещества, не содержащие цианогруппу (бифентрин, перметрин и др.). Воздействуя на организм животных, они вызывают тремор, гиперактивность, возбуждение (агрессивное поведение), мышечные контрактуры. Особенностями токсического действия пиретроидов ІІ типа – цианопиретроидов (альфа-циперметрин, бета-циперметрин, циперметрин, дельтаметрин, эсфенвалерат и др.) являются судороги и рецидивирующие судорожные припадки, гиперсаливация, хореатетозы, гиперкинезы[2].Электрофизиологические экспериментальные исследования говорят о том, что действие пиретроидов вызывает функциональные изменения постсинаптической нейрональной мембраны, вещества воздействуют на хемовозбудимые ионные каналы, обладают достаточно высоким сродством к никотиновым ацетилхолиновым рецепторам. Цианосодержащие пиретроиды при взаимодействии с рецепторами гамма-аминомасляной кислоты (ГАМК) в синаптосомах мозга, вызывают функциональные нарушения в работе экстрапирамидной системы и спинальных промежуточных нейронов[2].
Острые отравления
проявляются как головная боль, жжение и зуд кожи лица, головокружениие, общая слабость, в первые 2–3 суток повышении температуры тела до 38–39°С[2].Классы опасности
. Препараты на основе пиретроидных соединений относят ко 2 и 3 классам опасности для человека и 1, 2 и 3 для пчел[4].Пиретроиды ошибочно называют перетроидами и перитроидами. (прим. ред)
2. Балан Г.М., Иванова С.И. и др. Клинические проявления, лечение и отдаленные последствия острых отравлений синтетическими пиретроидами. УДК 615,9;632.95;616.8
3. Белов Д.А. Химические методы и средства защиты растений в лесном хозяйстве и озеленении: Учебное пособие для студентов. –М.: МГУЛ, 2003. – 128 с
4. Государственный каталог пестицидов и агрохимикатов, разрешенных к применению на территории Российской Федерации, 2024 год. Министерство сельского хозяйства Российской Федерации (Минсельхоз России)
5. Зинченко В.А. Химическая защита растений: средства, технология и экологическая безопасность. – М.: Колос С, 2005. – 232 с.
6. Мельников Н.Н. Пестициды. Химия, технология и применение. - М.: Химия, 1987. 712 с.
7. Пиретроиды – новая группа инсектицидов для борьбы с вредителями хлопчатника: Обзоринформ./УзНИИНТИ Ташкент, 1984.
8. Попов С.Я. Основы химической защиты растений. Попов С.Я., Дорожкина Л.А., Калинин В.А./ Под ред. профессора С.Я Попова. - М.: Арт-Лион, 2003. - 208 с.
9. Рекомендации по диагностике, лечению и профилактике отравлений животных синтетическими пиретроидами. Москва, ФГНУ «Росинформагротех», 2007.
10. Суворов А.В. справочник по клинической токсикологии. Нижний Новогород: Изд-во НГМА, 1996.
11. Ткачев А.В. Пиретроидные инсектициды – аналоги природных защитных веществ растений. Соровский образовательный журнал, том 8, №2, 2004.
Буклет препарата «Калипсо». BayerCropScience, 2011 год.
14.
Fly killer, by robynejay's , по лицензии CC BY-NC-SA



